لتنزيل هذه الصفحة أو طباعتها بلغة مختلفة، اختر لغتك من القائمة المنسدلة الموجودة في الجزء العلوي الأيسر أولاً.

ورقة موقف IAOMT بشأن تجاويف عظم الفك البشري
رئيس لجنة أمراض عظم الفك: تيد ريس، DDS، MAGD، NMD، FIAOMT
كارل أندرسون، DDS، MS، NMD، FIAOMT
باتريشيا بيروب، DMD، MS، CFMD، FIAOMT
جيري بوكوت ، دس ، إم إس دي
تيريزا فرانكلين، دكتوراه
جاك كال، DMD، FAGD، MIAOMT
كودي كريجل، DDS، NMD، FIAOMT
سوشما لافو، DDS، FIAOMT
تيفاني شيلدز، DMD، NMD، FIAOMT
مارك ويسنيوسكي، DDS، FIAOMT
تود اللجنة أن تعرب عن تقديرها لمايكل جوسويلر، DDS، MS، NMD، ميغيل ستانلي، DDS وستيوارت نونالي، DDS، MS، FIAOMT، NMD لانتقاداتهم لهذه الورقة. ونود أيضًا أن نشيد بالمساهمات والجهود القيمة التي بذلها الدكتور نونالي في تجميع ورقة الموقف لعام 2014. لقد كان عمله واجتهاده وممارسته بمثابة العمود الفقري لهذه الورقة المحدثة.
تمت الموافقة عليه من قبل مجلس إدارة IAOMT في سبتمبر 2023
جدول المحتويات
التصوير المقطعي المحوسب بالشعاع المخروطي (CBCT)
المؤشرات الحيوية والفحص النسيجي
اعتبارات متطورة لأغراض التشخيص
مراجع حسابات
الملحق الأول نتائج مسح IAOMT 2
التذييل الثاني نتائج مسح IAOMT 1
التذييل الثالث الصور
الشكل 1: تنخر العظم التنكسي الدهني في عظم الفك (FDOJ)
الشكل 2: السيتوكينات في FDOJ مقارنة بالضوابط الصحية
الشكل 3: الإجراء الجراحي لFDOJ خلف الرحى
الشكل 4: الكشط والأشعة السينية المقابلة لـ FDOJ
أفلام مقاطع فيديو لجراحة عظم الفك لدى المرضى
على مدى العقد الماضي كان هناك وعي متزايد بين الجمهور ومقدمي الرعاية الصحية بوجود صلة بين صحة الفم والصحة الجهازية. على سبيل المثال، أمراض اللثة هي عامل خطر لكل من مرض السكري وأمراض القلب. كما تم أيضًا إثبات وجود علاقة ذات أهمية كبيرة وبحث متزايد بين أمراض عظم الفك والصحة العامة والحيوية للفرد. كان استخدام طرائق التصوير المتقدمة تقنيًا مثل التصوير المقطعي المحوسب المخروطي (CBCT) فعالاً في تحديد أمراض عظم الفك، مما أدى إلى تحسين القدرات التشخيصية وتحسين القدرة على تقييم نجاح التدخلات الجراحية . أدت التقارير العلمية والدراما الوثائقية ووسائل التواصل الاجتماعي إلى زيادة الوعي العام بهذه الأمراض، خاصة بين الأفراد الذين يعانون من حالات عصبية أو جهازية مزمنة غير مبررة والتي تفشل في الاستجابة للتدخلات الطبية أو طب الأسنان التقليدية.
تأسست الأكاديمية الدولية لطب الفم وعلم السموم (IAOMT) على الاعتقاد بأن العلم يجب أن يكون الأساس الذي يتم عليه اختيار واستخدام جميع طرق التشخيص والعلاج. مع وضع هذه الأولوية في الاعتبار، فإننا 1) نقدم هذا التحديث لورقة موقف تنخر العظم في عظم الفك IAOMT لعام 2014، و2) نقترح، بناءً على الملاحظة النسيجية، اسمًا أكثر دقة من الناحية العلمية والطبية للمرض، على وجه التحديد، مرض نقص تروية النخاع المزمن عظم الفك (CIMDJ). يصف CIMDJ حالة العظام التي تتميز بموت المكونات الخلوية للعظم الإسفنجي، نتيجة لانقطاع إمدادات الدم. طوال تاريخها، تمت الإشارة إلى ما نشير إليه باسم CIMDJ من خلال العديد من الأسماء والمختصرات المدرجة في الجدول 1 وسيتم مناقشتها بإيجاز أدناه.
الهدف والغرض من هذه الأكاديمية والورقة هو توفير العلوم والأبحاث والملاحظات السريرية للمرضى والأطباء لاتخاذ قرارات مستنيرة عند النظر في آفات CIMDJ، والتي غالبًا ما يشار إليها باسم تجاويف عظم الفك. تم إعداد هذه الورقة البحثية لعام 2023 في جهد مشترك ضم أطباء وباحثين وأخصائي أمراض عظام الفك البارز، الدكتور جيري بوكوت، بعد مراجعة أكثر من 270 مقالًا.
لا توجد في أي عظمة أخرى احتمالية التعرض للصدمات والالتهابات كبيرة كما هي الحال في عظام الفك. تظهر مراجعة الأدبيات المتعلقة بموضوع تجاويف عظم الفك (أي CIMDJ) أن هذه الحالة قد تم تشخيصها وعلاجها والبحث فيها منذ ستينيات القرن التاسع عشر. في عام 1860 قدم الدكتور إتش آر نويل عرضا بعنوان محاضرة عن تسوس ونخر العظام في كلية بالتيمور لجراحة الأسنان، وفي عام 1901 تمت مناقشة تجاويف عظم الفك بشكل مطول بواسطة ويليام سي. باريت في كتابه المدرسي بعنوان، أمراض الفم وممارستها: كتاب مدرسي لاستخدام الطلاب في كليات طب الأسنان ودليل لممارسي طب الأسنان. قام جي في بلاك، الذي يُشار إليه غالبًا بأب طب الأسنان الحديث، بتضمين قسم في كتابه المدرسي لعام 1915، بعنوان "علم أمراض الأسنان الخاصة"، لوصف "المظهر المعتاد والعلاج" لما وصفه بنخر عظم الفك (JON).
بدا أن البحث عن تجاويف عظم الفك قد توقف حتى السبعينيات عندما بدأ آخرون في البحث في هذا الموضوع، باستخدام مجموعة متنوعة من الأسماء والتسميات، ونشر المعلومات المتعلقة به في الكتب المدرسية الحديثة لعلم أمراض الفم. على سبيل المثال، في عام 1970، لاحظ بوكوت وآخرون التهابًا داخل العظم لدى المرضى الذين يعانون من آلام الوجه المزمنة والشديدة (العدد = 1992) وصاغوا مصطلح "نخر العظم التجويف المسبب للألم العصبي"، أو NICO. على الرغم من أن بوكوت وآخرين لم يعلقوا على مسببات المرض، فقد خلصوا إلى أنه من المحتمل أن الآفات تسببت في ألم عصبي مزمن في الوجه مع سمات محلية فريدة: تكوين تجويف داخل العظم ونخر العظام طويل الأمد مع الحد الأدنى من الشفاء. في دراسة سريرية للمرضى الذين يعانون من الألم العصبي الثلاثي التوائم (العدد = 135) والألم العصبي الوجهي (العدد = 38)، أظهر راتنر وآخرون أيضًا أن جميع المرضى تقريبًا لديهم تجاويف في العظام السنخية وعظام الفك. كانت التجاويف، التي يبلغ قطرها أحيانًا أكثر من سنتيمتر واحد، موجودة في مواقع قلع الأسنان السابقة ولم يكن من الممكن اكتشافها بشكل عام بواسطة الأشعة السينية.

 توجد مجموعة متنوعة من المصطلحات الأخرى لما نسميه CIMDJ في الأدبيات. يتم سرد هذه في الجدول 1 ومناقشتها بإيجاز هنا. صاغ آدامز وآخرون مصطلح التهاب العظم والنقي الليفي المزمن (CFO) في ورقة موقف عام 2014. كانت ورقة الموقف نتيجة لاتحاد متعدد التخصصات من الممارسين من مجالات طب الفم، وعلاج الجذور، وعلم أمراض الفم، وعلم الأعصاب، وأمراض الروماتيزم، وطب الأنف والأذن والحنجرة، وأمراض اللثة، والطب النفسي، وأشعة الفم والوجه والفكين، والتخدير، وطب الأسنان العام، والطب الباطني، وإدارة الألم. . كان تركيز المجموعة هو توفير منصة متعددة التخصصات لعلاج الأمراض المرتبطة بالرأس والرقبة والوجه. ومن خلال الجهود الجماعية لهذه المجموعة، وعمليات البحث المكثفة في الأدبيات والمقابلات مع المرضى، ظهر نمط سريري متميز، والذي أشاروا إليه باسم المدير المالي. وأشاروا إلى أن هذا المرض غالبًا ما لا يتم تشخيصه بسبب أمراضه المصاحبة لحالات جهازية أخرى. وأشارت هذه المجموعة إلى الروابط المحتملة بين المرض والقضايا الصحية الجهازية والحاجة إلى فريق من الأطباء لتشخيص المريض وعلاجه بشكل صحيح.
توجد مجموعة متنوعة من المصطلحات الأخرى لما نسميه CIMDJ في الأدبيات. يتم سرد هذه في الجدول 1 ومناقشتها بإيجاز هنا. صاغ آدامز وآخرون مصطلح التهاب العظم والنقي الليفي المزمن (CFO) في ورقة موقف عام 2014. كانت ورقة الموقف نتيجة لاتحاد متعدد التخصصات من الممارسين من مجالات طب الفم، وعلاج الجذور، وعلم أمراض الفم، وعلم الأعصاب، وأمراض الروماتيزم، وطب الأنف والأذن والحنجرة، وأمراض اللثة، والطب النفسي، وأشعة الفم والوجه والفكين، والتخدير، وطب الأسنان العام، والطب الباطني، وإدارة الألم. . كان تركيز المجموعة هو توفير منصة متعددة التخصصات لعلاج الأمراض المرتبطة بالرأس والرقبة والوجه. ومن خلال الجهود الجماعية لهذه المجموعة، وعمليات البحث المكثفة في الأدبيات والمقابلات مع المرضى، ظهر نمط سريري متميز، والذي أشاروا إليه باسم المدير المالي. وأشاروا إلى أن هذا المرض غالبًا ما لا يتم تشخيصه بسبب أمراضه المصاحبة لحالات جهازية أخرى. وأشارت هذه المجموعة إلى الروابط المحتملة بين المرض والقضايا الصحية الجهازية والحاجة إلى فريق من الأطباء لتشخيص المريض وعلاجه بشكل صحيح.
وقد لوحظت أيضًا آفات تجويف عظم الفك عند الأطفال. في عام 2013، وصف أوبل وزملاؤه الآفات لدى الأطفال وصاغوا مصطلح التهاب العظم والنقي المزمن الفكي السفلي (JMCO). اقترحت هذه المجموعة إمكانية استخدام البايفوسفونيت عن طريق الوريد (IV) كعلاج لهؤلاء الأطفال. في عام 2016، نشر بادوا وآخرون دراسة تصف التهاب العظم الالتهابي العقيم البؤري في عظام الفك لدى مرضى الأطفال. لقد وصفوا الآفة بالتهاب العظم والنقي المزمن غير البكتيري لدى الأطفال (CNO).
منذ عام 2010، قام الدكتور يوهان ليتشنر، المؤلف والباحث الأكثر نشرًا في مجال آفات تجويف عظم الفك، وآخرون بالبحث في علاقة هذه الآفات بإنتاج السيتوكينات، وخاصة السيتوكينات الالتهابية RANTES (المعروف أيضًا باسم CCL5). استخدم الدكتور ليشنر مصطلحات مختلفة لوصف هذه الآفات التي شملت NICO المذكورة سابقًا ولكن أيضًا تنخر العظم الإقفاري العقيم في عظم الفك (AIOJ)، ونخر العظم التنكس الدهني في عظم الفك (FDOJ). يعتمد وصفه/تسميته على المظهر الجسدي و/أو الحالة المرضية التي يتم ملاحظتها سريريًا أو أثناء العملية الجراحية.
هناك الآن حاجة لتوضيح مرض آخر تم تحديده مؤخرًا في عظم الفك والذي يختلف عن موضوع هذه الورقة ولكنه قد يكون مربكًا لأولئك الذين يبحثون في آفات التجويف. هذه هي آفات عظمية في الفك تنشأ نتيجة استخدام المستحضرات الصيدلانية. تتميز الآفات بشكل أفضل بفقدان إمدادات الدم مع عزل العظام بشكل لا يمكن السيطرة عليه. تم تسمية هذه الآفات باسم تقرح الفم مع عزل العظام (OUBS) بواسطة Ruggiero et al في ورقة موقف لـ الرابطة الأمريكية لجراحي الفم والوجه والفكين (AAOMS)، وكذلك بواسطة Palla et al، في مراجعة منهجية. نظرًا لأن هذه المشكلة مرتبطة باستخدام دواء واحد أو عدة مستحضرات صيدلانية، فإن IAOMT ترى أن أفضل وصف لهذا النوع من الآفة هو تنخر عظم الفك المرتبط بالأدوية (MRONJ). لن تتم مناقشة MRONJ في هذه الورقة نظرًا لأن مسبباتها وأساليب علاجها تختلف عن تلك التي نشير إليها باسم CIMDJ، وقد تمت دراستها على نطاق واسع سابقًا.
أدى الاستخدام الشائع بشكل متزايد للصور الشعاعية المقطعية المخروطية (CBCT) من قبل العديد من ممارسي طب الأسنان إلى زيادة في ملاحظة التجاويف داخل النخاع التي نشير إليها باسم CIMDJ، والتي تم التغاضي عنها سابقًا وبالتالي تجاهلها. والآن بعد أن تم التعرف على هذه الآفات والشذوذات بسهولة أكبر، أصبح من مسؤولية مهنة طب الأسنان تشخيص المرض وتقديم توصيات العلاج والرعاية.
إن تقدير وتحديد وجود CIMDJ هو نقطة البداية لفهمه. بغض النظر عن الأسماء والمختصرات العديدة التي ارتبطت بعلم الأمراض، فإن وجود عظم نخري أو ميت في المكون النخاعي لعظم الفك أمر راسخ.
عند ملاحظة هذه العيوب العظمية أثناء الجراحة فإنها تظهر نفسها بطرق عديدة. أفاد بعض الممارسين أن أكثر من 75% من الآفات مجوفة تمامًا أو مملوءة بأنسجة ناعمة ذات لون بني رمادي ومنزوعة المعادن/الأورام الحبيبية، غالبًا مع مادة زيتية صفراء (كيسات زيتية) موجودة في المناطق المعيبة مع تشريح العظام الطبيعي المحيط. أفاد آخرون عن وجود تجاويف ذات كثافة عظمية قشرية متفاوتة والتي عند فتحها، يبدو أنها تحتوي على بطانات بمواد ليفية سوداء أو بنية أو رمادية. لا يزال البعض الآخر يشير إلى تغيرات جسيمة توصف بشكل مختلف بأنها "شجاعة" و"مثل نشارة الخشب" و"تجاويف مجوفة" و"جافة" مع تصلب عرضي وصلابة تشبه الأسنان في جدران التجويف. عند الفحص النسيجي، تبدو هذه الآفات مشابهة للنخر الذي يحدث في عظام أخرى من الجسم وتختلف نسيجيًا عن التهاب العظم والنقي (انظر الشكل 1). تم تضمين صور إضافية توضح مرض CIMDJ، وبعضها ذو طبيعة تصويرية، في الملحق الثالث في نهاية هذه الوثيقة.
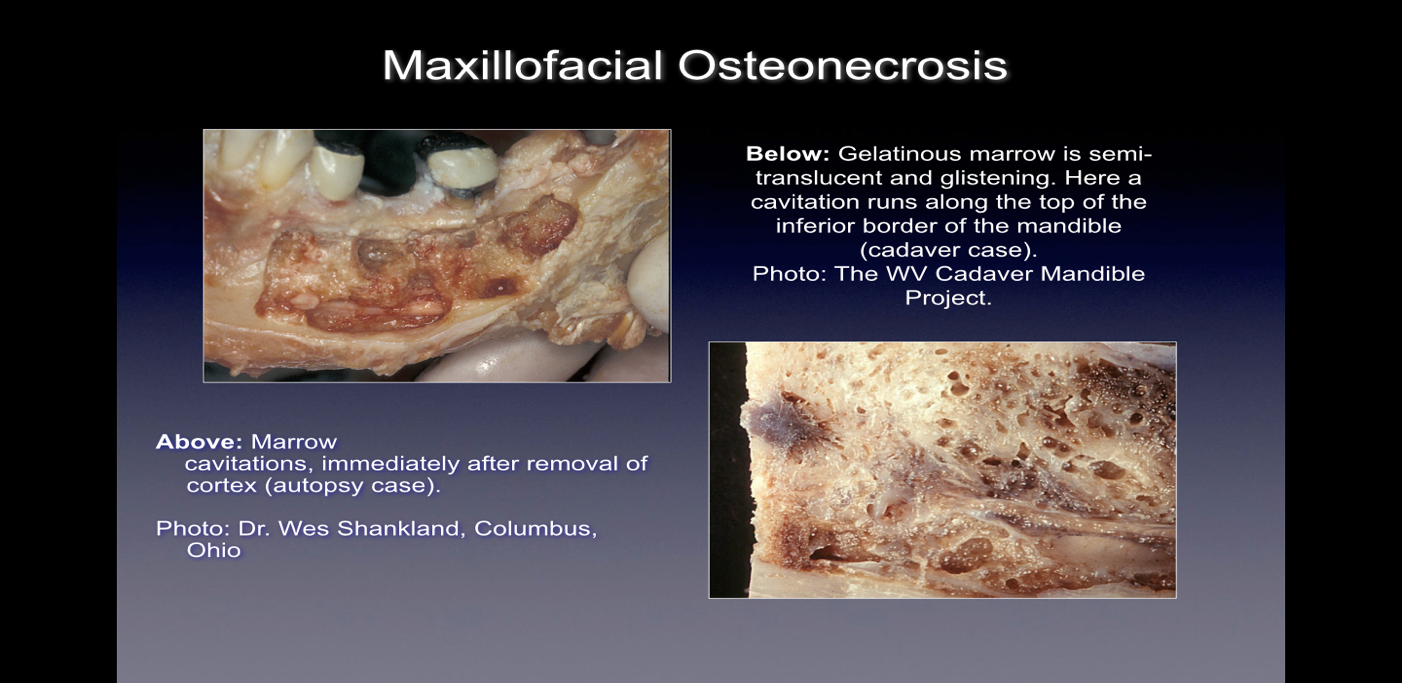
الشكل 1 صور CIMDJ مأخوذة من جثة
مثل غيرهم من ممارسي الرعاية الصحية، يستخدم أطباء الأسنان عملية منظمة تستخدم أساليب وطرق مختلفة لتشخيص آفات التجويف. قد تتكون هذه من إجراء فحص بدني يتضمن أخذ التاريخ الصحي، وتقييم الأعراض، والحصول على سوائل الجسم لإجراء الاختبارات المعملية، والحصول على عينات الأنسجة للخزعة والاختبارات الميكروبيولوجية (أي اختبار وجود مسببات الأمراض). غالبًا ما يتم استخدام تقنيات التصوير، مثل CBCT. في المرضى الذين يعانون من اضطرابات معقدة لا تتبع دائمًا نمطًا أو تتناسب مع ترتيب نموذجي لأعراض معقدة، يمكن أن تتطلب عملية التشخيص تحليلًا أكثر تفصيلاً والذي قد يؤدي في البداية فقط إلى تشخيص تفريقي. ويرد أدناه وصف موجز للعديد من طرق التشخيص هذه.
التصوير المقطعي المحوسب بالشعاع المخروطي (CBCT)
تقنيات التشخيص الموصوفة في وقت مبكر من عام 1979 من قبل راتنر وزملائه، باستخدام الجس والضغوط الرقمية، وحقن التخدير الموضعي التشخيصية، والنظر في التاريخ الطبي وموقع الألم المشع، مفيدة في تشخيص تجاويف عظم الفك. ومع ذلك، في حين أن بعض هذه الآفات تسبب الألم والتورم والاحمرار وحتى الحمى، فإن البعض الآخر لا يسبب ذلك. وبالتالي، غالبًا ما يكون من الضروري اتخاذ إجراء أكثر موضوعية، مثل التصوير.
عادةً لا يتم اكتشاف التجاويف في الأفلام الشعاعية القياسية ثنائية الأبعاد (ثنائية الأبعاد مثل المحيط القمي والبانورامية) التي تُستخدم عادةً في طب الأسنان. أظهر راتنر وزملاؤه أن 2% أو أكثر من العظام تحتاج إلى تعديل لإظهار التغييرات، وهذا ما تدعمه الأبحاث اللاحقة، كما هو موضح في الشكل 40. ويرتبط هذا بالقيود المتأصلة في التصوير ثنائي الأبعاد الذي يسبب التراكب. من الهياكل التشريحية، وإخفاء مجالات الاهتمام. في حالة العيوب أو الأمراض، خاصة في الفك السفلي، يمكن أن يكون تأثير إخفاء العظم القشري الكثيف على الهياكل الأساسية كبيرًا. لذلك، هناك حاجة إلى تقنيات تصوير متقدمة تقنيًا مثل CBCT، أو فحوصات Tech 2، أو التصوير بالرنين المغناطيسي (MRI)، أو التصوير بالموجات فوق الصوتية عبر السنخية (CaviTAU™®).
من بين تقنيات التصوير المختلفة المتوفرة، يعد CBCT الأداة التشخيصية الأكثر استخدامًا على نطاق واسع والتي يستخدمها أطباء الأسنان المشاركون في تشخيص أو علاج التجاويف، وبالتالي سنناقشها بعمق. حجر الزاوية في تكنولوجيا CBCT هو قدرتها على عرض الآفة محل الاهتمام في 3 أبعاد (أمامي، سهمي، إكليلي). لقد أثبت التصوير المقطعي المحوسب (CBCT) أنه طريقة موثوقة ودقيقة لتحديد وتقدير حجم ومدى العيوب داخل العظام في الفك مع تشويه أقل وتكبير أقل من الأشعة السينية ثنائية الأبعاد.
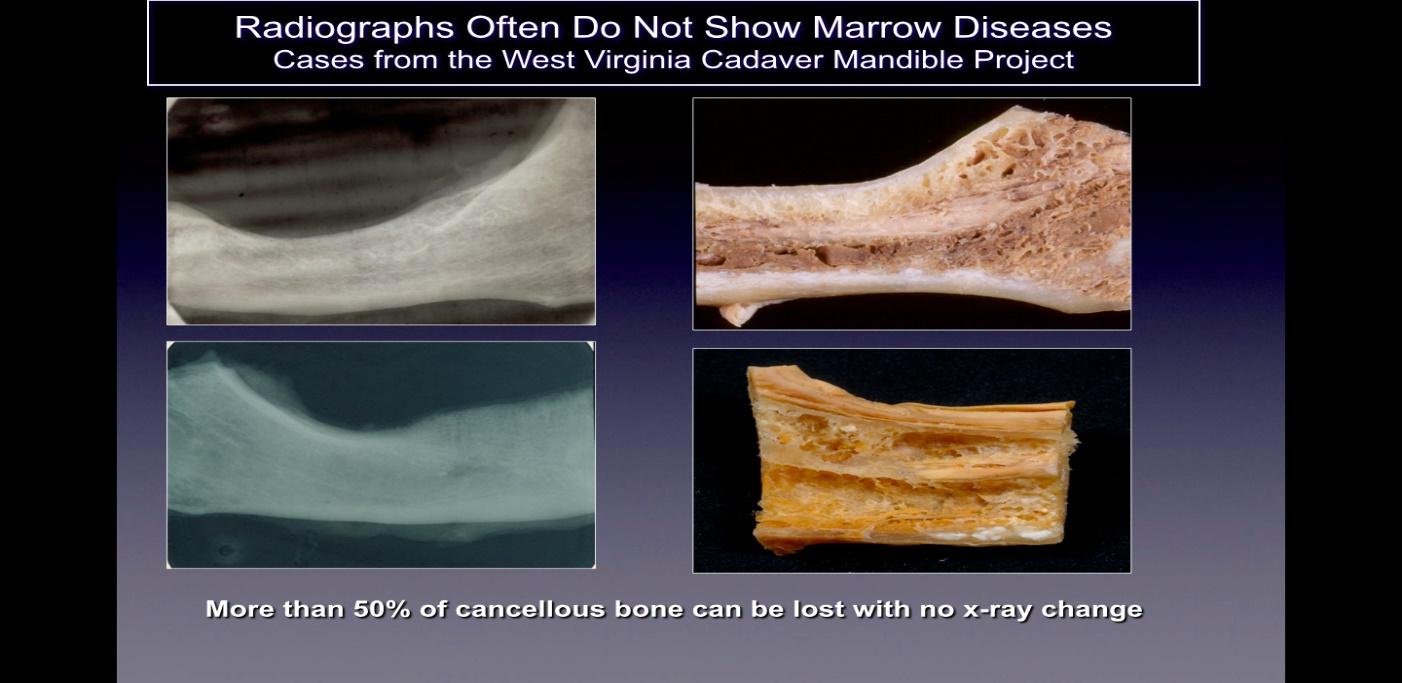
الشكل 2 تسمية توضيحية: على الجانب الأيسر تظهر صور شعاعية ثنائية الأبعاد لعظام الفك مأخوذة من الجثث التي تظهر
صحيح. على الجانب الأيمن من الشكل توجد صور لنفس عظام الفك تظهر تجويفًا نخريًا واضحًا.
الشكل مقتبس من بوكوت، 2014.
أظهرت الدراسات السريرية أن صور CBCT تساعد أيضًا في تحديد محتويات الآفة (المملوءة بالسوائل، أو الورم الحبيبي، أو الصلبة، وما إلى ذلك)، وربما تساعد في التمييز بين الآفات الالتهابية، والأورام السنية أو غير السنية، والخراجات، وغيرها من الأورام الحميدة أو الخبيثة. الآفات.
تستخدم البرامج التي تم تطويرها مؤخرًا والتي تم دمجها خصيصًا مع أنواع مختلفة من أجهزة CBCT وحدات Hounsfield (HU) التي تسمح بإجراء تقييم موحد لكثافة العظام . تمثل HU الكثافة النسبية لأنسجة الجسم وفقًا لمقياس المستوى الرمادي المعاير، استنادًا إلى قيم الهواء (-1000 HU)، والماء (0 HU)، وكثافة العظام (+1000 HU). الشكل 3 يصور وجهات نظر مختلفة لصورة CBCT الحديثة.
باختصار، أثبت CBCT فائدته في تشخيص وعلاج تجاويف عظم الفك من خلال:
- تحديد حجم ومدى وموضع الآفة ثلاثي الأبعاد؛
- تحديد مدى قرب الآفة من الهياكل التشريحية الحيوية القريبة الأخرى مثل
العصب السنخي السفلي، الجيب الفكي العلوي، أو جذور الأسنان المجاورة؛
- تحديد نهج العلاج: الجراحة مقابل غير الجراحية؛ و
- تقديم صورة متابعة لتحديد درجة الشفاء والحاجة المحتملة
لإعادة علاج الآفة.
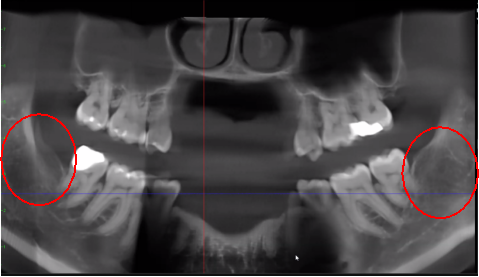
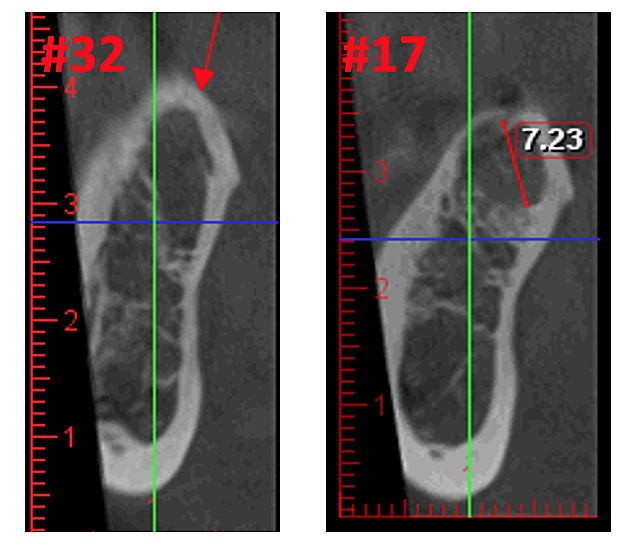
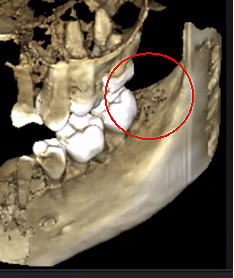
الشكل 3 تحسين وضوح صورة CBCT بفضل تكنولوجيا البرمجيات المحسنة، التي تقلل من الشوائب و"الضوضاء" التي يمكن أن تسببها زراعة الأسنان والترميمات المعدنية في الصورة. وهذا يسمح لطبيب الأسنان والمريض بتصور الآفة بسهولة أكبر. اللوحة العلوية عبارة عن منظر بانورامي لـ CBCT يُظهر الموقع الأيسر (#17) واليمين (#32) ومدى آفات التجويف لدى مريض تنخر عظم الفك. اللوحة اليسرى السفلية عبارة عن عرض سهمي لكل موقع. اللوحة اليمنى السفلية عبارة عن عرض ثلاثي الأبعاد للموقع رقم 3 يُظهر المسامية القشرية التي تغطي التجويف النخاعي. بإذن من الدكتور ريس.
نذكر هنا أيضًا بإيجاز جهاز الموجات فوق الصوتية، CaviTAU™®، الذي تم تطويره ويستخدم في أجزاء من أوروبا، خصيصًا لاكتشاف المناطق منخفضة الكثافة العظمية في عظام الفك العلوي والسفلي التي تشير إلى تجاويف عظم الفك. من المحتمل أن يكون جهاز التصوير بالموجات فوق الصوتية عبر السنخية (TAU-n) متساويًا بالمقارنة مع CBCT في اكتشاف عيوب نخاع عظم الفك، وله فائدة إضافية تتمثل في تعريض المريض لمستويات أقل بكثير من الإشعاع. هذا الجهاز غير متوفر حاليًا في الولايات المتحدة ولكنه قيد المراجعة من قبل إدارة الغذاء والدواء الأمريكية ويمكن أن يكون أداة التشخيص الأساسية المستخدمة في أمريكا الشمالية لعلاج CIMJD.
المؤشرات الحيوية والفحص النسيجي
بسبب الطبيعة الالتهابية لتجويفات عظم الفك، قام ليتشنر وباير في عام 2017 بالتحقيق في العلاقة المحتملة بين السيتوكينات المختارة والمرض. يتم تنظيم أحد السيتوكينات ذات الأهمية الخاصة عند التنشيط، ويتم التعبير عن الخلايا التائية الطبيعية وإفرازها (RANTES). يتم التعبير عن هذا السيتوكين، وكذلك عامل نمو الخلايا الليفية (FGF) -2، بكميات أكبر في الآفات التجويفية وفي المرضى الذين يعانون من CIMDJ. يقارن الشكل 4، الذي قدمه الدكتور ليشنر، مستويات RANTES في المرضى الذين يعانون من التجاويف (الشريط الأحمر، اليسار) مع المستويات في الضوابط الصحية (الشريط الأزرق)، مما يدل على مستويات أكبر بأكثر من 25 مرة في أولئك الذين يعانون من المرض. يستخدم Lechner et al طريقتين لقياس مستويات السيتوكينات. الأول هو قياس مستويات السيتوكينات بشكل نظامي من الدم (مختبر الحلول التشخيصية، الولايات المتحدة الأمريكية.). الطريقة الثانية هي أخذ خزعة مباشرة من الموقع المصاب عند الوصول إليها ليتم تقييمها من قبل أخصائي أمراض الفم. لسوء الحظ، في هذا الوقت، يتطلب أخذ عينات الأنسجة الموضعية معالجة وشحنًا معقدًا لم يتم تحقيقه بعد في المرافق غير البحثية، ولكنه قدم ارتباطات ثاقبة.
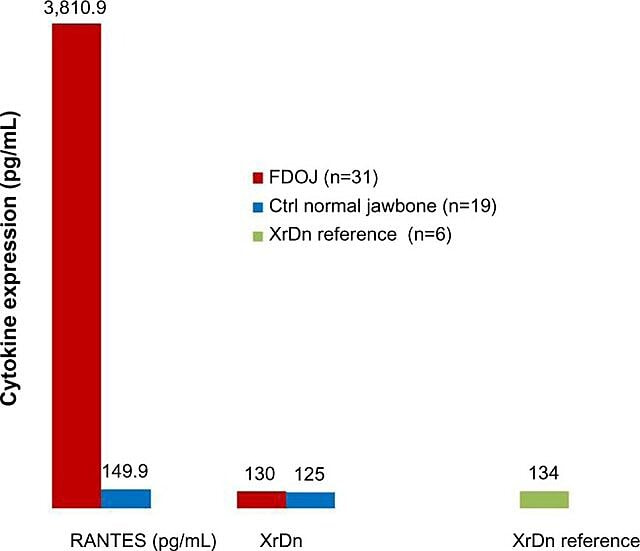
الشكل 4 توزيع RANTES في 31 حالة FDOJ و19 عينة من عظم الفك الطبيعي مقارنة بمرجع كثافة الأشعة السينية لكلا المجموعتين في المناطق المقابلة. الاختصارات: RANTES ، يتم تنظيمه عند التنشيط ، والخلايا التائية الطبيعية المعبر عنها والمفرزة (عزر CC) ligand 5 ؛ XrDn، كثافة الأشعة السينية؛ FDOJ، تنخر العظم التنكس الدهني في عظم الفك؛ ن، رقم؛ السيطرة، السيطرة. الشكل مقدم من الدكتور ليخنر. رقم الرخصة: CC BY-NC 3.0
اعتبارات متطورة لأغراض التشخيص
لقد تم إثبات وجود تجاويف في عظم الفك سريريًا. ومع ذلك، فإن التشخيص الواضح وأفضل الممارسات العلاجية تحتاج إلى مزيد من البحث. مع أخذ ذلك في الاعتبار، من الضروري أن نذكر بإيجاز بعض التقنيات المثيرة للاهتمام والتي يحتمل أن تكون ذات قيمة والتي يستخدمها بعض الممارسين.
ومن المسلم به أن التقييمات الفسيولوجية الإضافية ستكون أداة فحص وتشخيص قيمة. إحدى هذه الأدوات التي يستخدمها بعض الممارسين هي التصوير الحراري. يمكن ملاحظة النشاط الالتهابي المعمم من خلال قياس فروق الحرارة على سطح الرأس والرقبة. يعد التصوير الحراري آمنًا وسريعًا وقد تكون له قيمة تشخيصية مماثلة لتلك الخاصة بـ CBCT . العيب الكبير هو أنه يفتقر إلى التعريف، مما يجعل من الصعب تمييز هامش أو مدى الآفة.
يبحث بعض الممارسين في المظهر النشط للآفة باستخدام تقييم خط الطول بالوخز بالإبر (AMA) لتحديد تأثيره على خط الطاقة المقابل له. يعتمد هذا النوع من التقييم على الوخز بالإبر الكهربائي وفقًا لـ Voll (EAV). وقد تم تطوير هذه التقنية، التي تعتمد على الطب الصيني القديم ومبادئ الوخز بالإبر، ويتم تدريسها في الولايات المتحدة. تم استخدام الوخز بالإبر لتخفيف الألم وتعزيز الشفاء. وهو يعتمد على توازن تدفق الطاقة (أي تشي) عبر مسارات محددة للطاقة في الجسم. تربط هذه المسارات، أو خطوط الطول، أعضاء وأنسجة وعضلات وعظام معينة مع بعضها البعض. يستخدم الوخز بالإبر نقاطًا محددة جدًا على خط الطول للتأثير على صحة وحيوية جميع عناصر الجسم الموجودة على خط الطول هذا. تم استخدام هذه التقنية للكشف عن مرض عظم الفك، والذي عند حله يعالج أيضًا أمراضًا تبدو غير ذات صلة، مثل التهاب المفاصل أو متلازمة التعب المزمن. هذه التقنية تفسح المجال لمزيد من التحقيق (أي، يجب توثيق النتائج والحصول على البيانات الطولية ونشرها).
هناك العديد من العوامل الفردية التي تزيد من خطر الإصابة بتجويفات عظم الفك، ولكن عادة ما يكون الخطر متعدد العوامل. يمكن أن تكون المخاطر التي يتعرض لها الفرد إما تأثيرات خارجية، مثل العوامل البيئية أو تأثيرات داخلية، مثل ضعف وظيفة المناعة. يسرد الجدولان 2 و3 عوامل الخطر الخارجية والداخلية.


لاحظ أن الجدول 2، عوامل الخطر الداخلية، لا يشمل الاستعداد الوراثي. في حين يُعتقد أن التباينات الجينية تلعب دورًا، لم يتم تحديد أي اختلاف جيني واحد أو حتى مجموعة من الجينات كعامل خطر، ولكن التأثيرات الجينية محتملة . أظهرت مراجعة منهجية للأدبيات أجريت في عام 2019 أنه تم تحديد عدد من أشكال النوكليوتيدات الفردية، ولكن لا يوجد تكرار عبر الدراسات. وخلص الباحثون إلى أنه نظرا لتنوع الجينات التي أظهرت ارتباطات إيجابية مع التجاويف وعدم إمكانية تكرار الدراسات، فإن الدور الذي تلعبه الأسباب الوراثية يبدو معتدلا وغير متجانس. ومع ذلك، قد يكون من الضروري استهداف مجموعات سكانية معينة لتحديد الاختلافات الجينية. في الواقع، كما تم إثباته، فإن إحدى الآليات الفيزيولوجية المرضية الأكثر شيوعًا والأساسية لتلف العظام الإقفارية هي التخثر الزائد الناتج عن حالات فرط تخثر الدم، والتي عادة ما يكون لها أسس وراثية، كما وصفها بوكوت ولامارش (1999). يسرد الجدول 4 الذي قدمه الدكتور بوكوت الحالات المرضية التي تنطوي على فرط تخثر الدم، وتقدم الفقرات الثلاث التالية نظرة عامة على بعض النتائج التي توصل إليها الدكتور بوكوت والتي قدمها في دوره كمدير للأبحاث في مركز الوجه والفكين للتعليم والأبحاث.
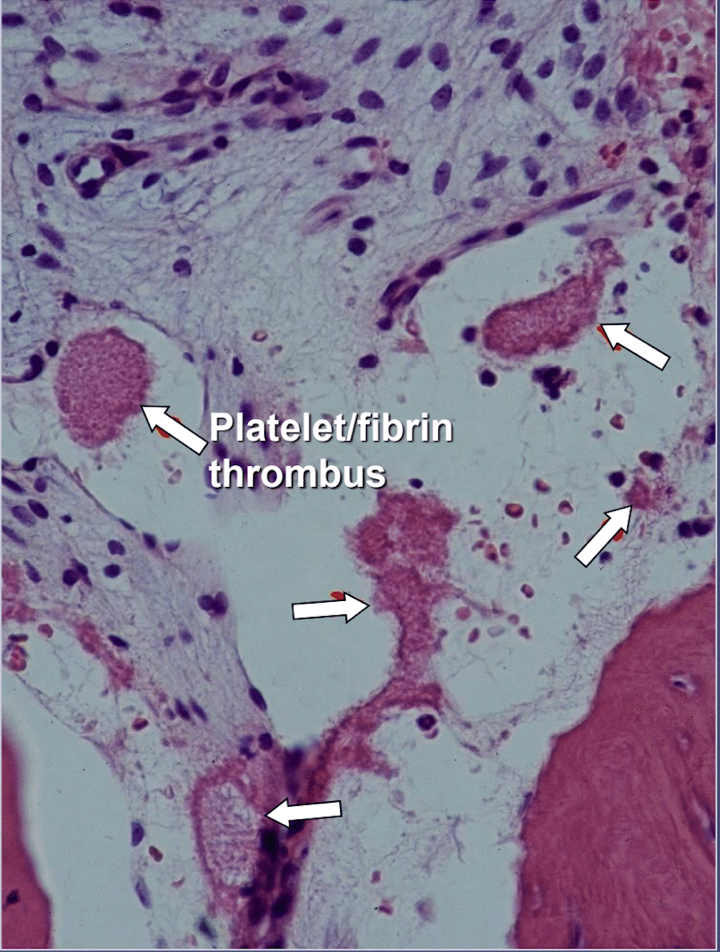
في تجاويف عظم الفك هناك دليل واضح على نخر العظم الإقفاري، وهو مرض نخاع العظم حيث يصبح العظم نخريًا بسبب الحرمان من الأكسجين والمغذيات. كما ذكرنا سابقًا، يمكن أن تتفاعل العديد من العوامل لتسبب التجاويف، ويعاني ما يصل إلى 80% من المرضى من مشكلة، عادة ما تكون موروثة، تتمثل في الإفراط في إنتاج جلطات الدم في الأوعية الدموية. لا يتم الكشف عن هذا المرض عادة خلال اختبارات الدم الروتينية. العظام معرضة بشكل خاص لمشكلة فرط تخثر الدم وتطور أوعية دموية متوسعة بشكل كبير. زيادة الضغوط الداخلية، والمؤلمة في كثير من الأحيان؛ ركود الدم وحتى النوبات. يمكن اقتراح مشكلة فرط تخثر الدم هذه من خلال وجود تاريخ عائلي للإصابة بالسكتة الدماغية والنوبات القلبية في سن مبكرة (أقل من 55 عامًا)، أو استبدال مفصل الورك أو "التهاب المفاصل" (خاصة في سن مبكرة)، أو تنخر العظم (خاصة في سن مبكرة)، أو النزف العميق. تجلط الأوردة، الصمات الرئوية (جلطات دموية في الرئتين)، تجلط الوريد الشبكي (جلطات في شبكية العين) والإجهاض المتكرر. يعاني الفك من مشكلتين محددتين مع هذا المرض: 2) بمجرد تعرضه للتلف، يصبح العظم المريض غير قادر على تحمل العدوى منخفضة الدرجة من بكتيريا الأسنان واللثة؛ و1) قد لا يتعافى العظم من انخفاض تدفق الدم الناجم عن التخدير الموضعي الذي يستخدمه أطباء الأسنان أثناء علاج الأسنان. يقدم الشكل 2 رؤية مجهرية للخثرة داخل الأوعية الدموية.
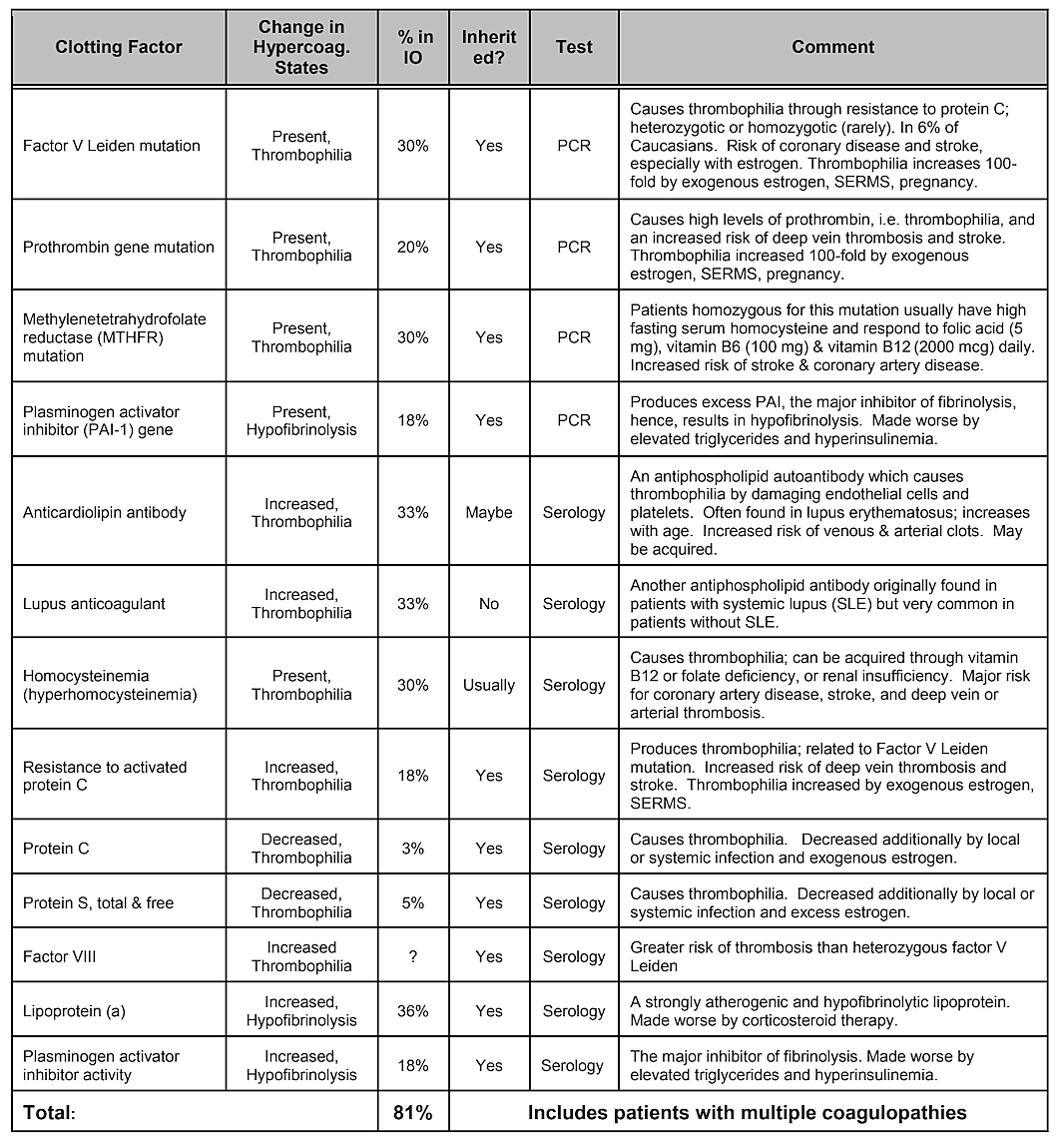
الجدول 4 حالات المرض التي تنطوي على فرط تخثر الدم. أربعة من كل خمسة مرضى تجويف عظم الفك لديهم واحدة من هذه التجلطات
مشاكل العوامل.
بغض النظر عن السبب الكامن وراء فرط تخثر الدم، فإن العظم يتطور إما نخاع ليفي (يمكن أن تعيش الألياف في المناطق المتعطشة للمغذيات)، أو نخاع دهني ميت ("العفن الرطب")، أو نخاع جاف جدًا، وفي بعض الأحيان مصنوع من الجلد ("العفن الجاف"). ) أو مساحة نخاع مجوفة تمامًا ("التجويف").
يمكن أن تتأثر أي عظمة، لكن الوركين والركبتين والفكين هي الأكثر إصابة. الألم غالبا ما يكون شديدا ولكن حوالي 1/3rd من المرضى لا يشعرون بالألم. ويواجه الجسم صعوبة في شفاء نفسه من هذا المرض و2/3طلقة من الحالات تتطلب الاستئصال الجراحي للنخاع التالف، عادة عن طريق الكشط بالمكشطة. سوف تقضي الجراحة على المشكلة (والألم) في حوالي 3/4تي إتش إس من المرضى الذين يعانون من تورط الفك، على الرغم من تكرار العمليات الجراحية، وعادة ما تكون إجراءات أصغر من الأولى، تكون مطلوبة في 40٪ من المرضى، وأحيانًا في أجزاء أخرى من الفكين، لأن المرض كثيرًا ما يكون له آفات "تخطي" (أي مواقع متعددة في الفك). نفس العظام أو ما شابهها)، مع وجود نخاع طبيعي بينهما. أكثر من نصف مرضى الورك سيصابون في النهاية بالمرض في الورك المقابل. أكثر من 1/3rd من مرضى عظام الفك يصابون بالمرض في الأرباع الأخرى من الفك. في الآونة الأخيرة، وجد أن 40% من المرضى الذين يعانون من تنخر العظم في الورك أو الفك يستجيبون لمضادات تخثر الدم باستخدام الهيبارين منخفض الوزن الجزيئي (لوفينوكس) أو الكومادين مع زوال الألم وشفاء العظام.
الشكل 5 عرض مجهري للجلطات الدموية داخل الأوعية الدموية
إذا كنت تبحث عن نهج غير دوائي لتقليل خطر فرط تخثر الدم، فيمكن التفكير في استخدام الإنزيمات التكميلية مثل ناتوكيناز أو لومبروكيناز الأكثر قوة وكلاهما له خصائص حال للفبرين ومضادة لتخثر الدم. بالإضافة إلى ذلك، ينبغي استبعاد حالات نقص النحاس، المرتبطة بخلل في تخثر الدم، بسبب زيادة خطر فرط تخثر الدم الذي لوحظ في المرضى الذين يعانون من تجاويف عظم الفك.
يشمل وجود تجاويف عظم الفك والأمراض المرتبطة بها بعض الأعراض المحددة ولكنه غالبًا ما يتضمن أيضًا بعض الأعراض الجهازية غير المحددة. وبالتالي، ينبغي التعامل مع تشخيصه وعلاجه بدراسة شاملة من قبل فريق الرعاية. إن الإنجازات الفريدة والرائدة التي ظهرت إلى النور منذ ورقة موقف IAOMT 2014 هي حل الحالات الالتهابية المزمنة التي تبدو غير ذات صلة بعد علاج التجويف. سواء كانت الأمراض الجهازية ذات طبيعة مناعية ذاتية أو التهابات تحدث بطريقة أخرى، فقد تم الإبلاغ عن تحسينات كبيرة، بما في ذلك تحسن السرطان. إن مجموعة الأعراض المرتبطة بهذه الآفات فردية للغاية وبالتالي لا يمكن تعميمها أو التعرف عليها بسهولة. ولذلك، فإن IAOMT ترى أنه عندما يتم تشخيص إصابة المريض بتجويف في عظم الفك مع أو بدون ألم موضعي مرتبط، ويكون لديه أيضًا مرض جهازي آخر لم يكن منسوبًا في السابق إلى تجاويف عظم الفك، فإن المريض يحتاج إلى مزيد من التقييم لتحديد ما إذا كان المرض مرتبطًا أو نتيجة للمرض. قامت IAOMT باستبيان أعضائها لمعرفة المزيد حول الأعراض/ الأمراض الجهازية التي يتم علاجها بعد جراحة التجويف. وترد النتائج في الملحق الأول.
يبدو أن وجود السيتوكينات المتولدة في الآفات النخرية ضعيفة الأوعية الدموية في تجاويف عظم الفك يعمل بمثابة تركيز للسيتوكينات الالتهابية التي تحافظ على مناطق الالتهاب الأخرى نشطة و/أو مزمنة. من المأمول والمتوقع حدوث تخفيف أو على الأقل تحسن من آلام الفك الموضعية بعد العلاج، ولكن هذه النظرية البؤرية للالتهاب، والتي سيتم مناقشتها بالتفصيل أدناه، قد تفسر سبب وجود العديد من الأمراض التي تبدو "غير مرتبطة" والتي لها روابط بحالات التهابية مزمنة. يتم تقليلها أيضًا مع علاج التجويف.
دعمًا للاستنتاجات التي تم التوصل إليها في ورقة موقف IAOMT لعام 2014 التي تربط تجاويف عظم الفك والأمراض الجهازية، تُظهر الأبحاث والدراسات السريرية التي نشرها مؤخرًا ليشنر وفون بير وآخرون أن آفات تجويف عظم الفك تحتوي على ملف تعريف سيتوكين محدد لم يتم رؤيته في أمراض العظام الأخرى . عند مقارنتها بعينات عظم الفك السليمة، تظهر أمراض التجويف باستمرار انتفاخًا قويًا لعامل نمو الخلايا الليفية (FGF-2)، ومضاد مستقبلات Interleukin 1 (Il-1ra)، والأهم من ذلك، RANTES . RANTES، المعروف أيضًا باسم CCL5 (cc motif Ligand 5) تم وصفه على أنه سيتوكين كيميائي له تأثير قوي على الالتهاب. لقد ثبت أن هذه المركبات الكيميائية تتدخل في عدة مراحل من الاستجابة المناعية وتشارك بشكل كبير في العديد من الحالات المرضية والالتهابات. أظهرت الدراسات أن RANTES متورط في العديد من الأمراض الجهازية مثل التهاب المفاصل ومتلازمة التعب المزمن والتهاب الجلد التأتبي والتهاب الكلية والتهاب القولون والثعلبة واضطرابات الغدة الدرقية وتعزيز التصلب المتعدد ومرض باركنسون. علاوة على ذلك، ثبت أن RANTES يسبب تسارعًا في نمو الورم.
كما أن عوامل نمو الخلايا الليفية متورطة في تجاويف عظم الفك. تعتبر عوامل نمو الخلايا الليفية، FGF-2، والمستقبلات المرتبطة بها، مسؤولة عن العديد من الوظائف الحيوية، بما في ذلك تكاثر الخلايا، والبقاء على قيد الحياة، والهجرة. كما أنها عرضة للاختطاف من قبل الخلايا السرطانية ولعب دور مسبب للسرطان في العديد من أنواع السرطان. على سبيل المثال، يعزز FGF-2 تطور الورم والسرطان في سرطان البروستاتا. بالإضافة إلى ذلك، أظهرت مستويات FGF-2 ارتباطًا مباشرًا بالتقدم والورم الخبيث وسوء تشخيص البقاء على قيد الحياة لدى مرضى سرطان القولون والمستقيم. بالمقارنة مع الأشخاص غير المصابين بالسرطان، فإن المرضى الذين يعانون من سرطان المعدة لديهم مستويات أعلى بكثير من FGF-2 في مصلهم. وقد تورطت هذه الرسائل الالتهابية في العديد من الأمراض الخطيرة سواء كانت ذات طبيعة التهابية أو سرطانية. على النقيض من RANTES/CCL5 وFGF-2، فقد ثبت أن IL1-ra يعمل كوسيط قوي مضاد للالتهابات، مما يساهم في عدم وجود علامات التهابية شائعة داخل بعض آفات التجويف .
تمت مقارنة المستويات المفرطة من RANTES وFGF-2 في آفات التجويف وربطها بالمستويات التي لوحظت في أمراض جهازية أخرى مثل التصلب الجانبي الضموري والتصلب المتعدد (ALS) والتهاب المفاصل الروماتويدي وسرطان الثدي. في الواقع، فإن مستويات هذه الرسائل المكتشفة في تجاويف عظم الفك أعلى منها في المصل والسائل النخاعي لدى مرضى التصلب الجانبي الضموري والتصلب المتعدد. أظهرت الأبحاث الحالية التي أجراها Lechner و von Baehr زيادة قدرها 26 ضعفًا في RANTES في آفات عظم الفك العظمي لدى مرضى سرطان الثدي. يقترح ليشنر وزملاؤه أن RANTES المشتق من التجويف قد يكون بمثابة مسرّع لتطور سرطان الثدي وتطوره.
كما ذكرنا سابقًا، هناك العديد من حالات تجاويف عظم الفك بدون أعراض. في هذه الحالات، لا يتم رؤية السيتوكينات الحادة المؤيدة للالتهابات مثل TNF-alpha و IL-6، بأعداد متزايدة في النتائج النسيجية المرضية لعينات التجويف. في هؤلاء المرضى، يرتبط غياب هذه السيتوكينات المؤيدة للالتهابات بمستويات عالية من مضادات مستقبلات السيتوكينات المضادة للالتهابات إنترلوكين 1 (Il-1ra). الاستنتاج المعقول هو أن الالتهاب الحاد المرتبط بتجويفات عظم الفك يخضع لسيطرة المستويات العالية من RANTES/FGF-2. ونتيجة لذلك، لإجراء التشخيص، يقترح ليخنر وفون بير عدم التركيز على وجود الالتهاب والنظر في مسار الإشارة، في المقام الأول عبر التعبير الزائد عن RANTES/FGF-2. تشير المستويات العالية من RANTES/FGF-2 لدى مرضى التجويف إلى أن هذه الآفات قد تسبب مسارات إشارات مسببة للأمراض مماثلة ومعززة بشكل متبادل للأعضاء الأخرى. يتم تنشيط الجهاز المناعي استجابةً لإشارات الخطر، والتي تثير مسارات جزيئية فطرية مختلفة تبلغ ذروتها في إنتاج السيتوكينات الالتهابية واحتمال تفعيل جهاز المناعة التكيفي. وهذا يدعم الفكرة والنظرية القائلة بأن تجاويف عظم الفك قد تكون بمثابة سبب أساسي للأمراض الالتهابية المزمنة عن طريق إنتاج RANTES/FGF-2 ويشرح أيضًا سبب عدم رؤية أو الشعور بالأعراض الحادة للالتهاب دائمًا من قبل المريض في آفات عظم الفك. أنفسهم. وبالتالي، فإن تجاويف عظم الفك وهذه الرسل المتورطة تمثل جانبًا تكامليًا للمرض الالتهابي وتكون بمثابة مسببات محتملة للمرض. قد تكون إزالة التجاويف مفتاحًا لعكس الأمراض الالتهابية. ويدعم ذلك ملاحظة انخفاض مستويات RANTES في الدم بعد التدخل الجراحي في 5 مرضى بسرطان الثدي (انظر الجدول 5). قد يوفر المزيد من البحث والاختبار لمستويات RANTES/CCL5 نظرة ثاقبة لهذه العلاقة. الملاحظات المشجعة هي التحسن في نوعية الحياة الذي حققه العديد من مرضى تجويف عظم الفك، سواء كان ذلك راحة في موقع العملية أو تقليل الالتهاب المزمن أو المرض في مكان آخر.
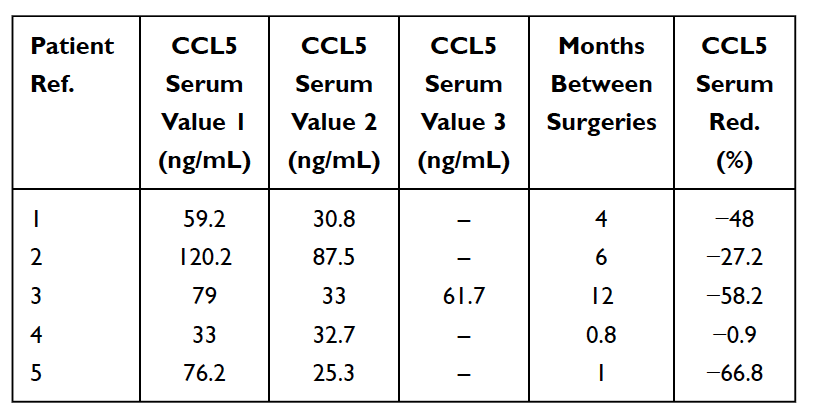
الجدول 5
التخفيض (الأحمر.) في RANTES / CCL5 في المصل في 5 مرضى سرطان الثدي الذين خضعوا لعملية جراحية لنخر العظم الدهني التنكسية في عظم الفك (FDOJ). الجدول مقتبس من
Lechner et al, 2021. تعبير عن تجويف عظم الفك RANTES/CCL5: دراسات حالة تربط الالتهاب الصامت في عظم الفك بنظرية المعرفة الخاصة بسرطان الثدي. سرطان الثدي: الأهداف والعلاج.
نظرًا لندرة الأدبيات المتعلقة بمعالجة آفات التجويف، قامت IAOMT بمسح أعضائها لجمع معلومات بخصوص الاتجاهات والعلاجات التي تتطور نحو "معيار الرعاية". وتتم مناقشة نتائج المسح بإيجاز في الملحق الثاني.
بمجرد تحديد موقع وحجم الآفات، تكون هناك حاجة إلى طرق العلاج. ترى IAOMT أنه من غير المقبول عمومًا ترك "عظام ميتة" في جسم الإنسان. يعتمد هذا على البيانات التي تشير إلى أن تجاويف عظم الفك يمكن أن تكون بؤر السيتوكينات الجهازية والسموم الداخلية لبدء عملية تدهور الصحة العامة للمريض.
في ظل الظروف المثالية، ينبغي إجراء خزعة لتأكيد تشخيص أي أمراض في عظم الفك واستبعاد الحالات المرضية الأخرى. بعد ذلك، من الضروري إجراء علاج لإزالة أو إزالة الأمراض المعنية وتحفيز إعادة نمو العظام الطبيعية والحيوية. في هذا الوقت، في الأدبيات التي راجعها النظراء، يبدو أن العلاج الجراحي الذي يتكون من استئصال العظم غير الحيوي المصاب هو العلاج المفضل لتجويف عظم الفك. يتضمن العلاج استخدام التخدير الموضعي، الأمر الذي يؤدي إلى اعتبار مهم. كان يُعتقد سابقًا أن أدوية التخدير المحتوية على الإبينفرين، والتي لها خصائص مضيق للأوعية، يجب تجنبها في المرضى الذين قد يكون لديهم بالفعل تدفق دم ضعيف مرتبط بحالتهم المرضية. ومع ذلك، في سلسلة من الدراسات الجزيئية، زاد التمايز العظمي مع استخدام الإبينفرين. ولذلك، يجب على الطبيب أن يحدد على أساس كل حالة على حدة ما إذا كان سيتم استخدام الإبينفرين أم لا، وإذا كان الأمر كذلك، فإن الكمية التي يجب استخدامها والتي ستعطي أفضل النتائج.
بعد التقشير الجراحي والكشط الشامل للآفة والري بمحلول ملحي طبيعي معقم، يتم تعزيز الشفاء عن طريق وضع طعوم الفيبرين الغنية بالصفائح الدموية (PRF) في الفراغ العظمي. إن استخدام مركزات الفيبرين الغنية بالصفائح الدموية في العمليات الجراحية ليس مفيدًا فقط من حيث التخثر، ولكن أيضًا من حيث إطلاق عوامل النمو على مدى فترة تصل إلى أربعة عشر يومًا بعد الجراحة. قبل استخدام طعوم PRF والعلاجات المساعدة الأخرى، حدث انتكاس لآفة النخر العظمي في عظم الفك بعد الجراحة في ما يصل إلى 40% من الحالات.
إن دراسة عوامل الخطر الخارجية المبينة في الجدول 2 تشير بقوة إلى أنه يمكن تجنب النتائج غير المواتية باستخدام التقنية الجراحية المناسبة والتفاعل بين الطبيب والمريض، خاصة في المجموعات السكانية المعرضة للإصابة. يُنصح بالتفكير في اعتماد تقنيات غير مؤلمة، وتقليل أو الوقاية من أمراض اللثة وغيرها من أمراض الأسنان، واختيار المعدات التي تسمح بتحقيق أفضل نتائج الشفاء. إن توفير تعليمات شاملة قبل وبعد العملية الجراحية للمريض، بما في ذلك المخاطر المرتبطة بتدخين السجائر، يمكن أن يساعد في تقليل النتائج السلبية.
مع الأخذ في الاعتبار القائمة الواسعة من عوامل الخطر المحتملة المدرجة في الجدولين 2 و3، يوصى بإجراء مشاورات مع فريق الرعاية الموسعة للمريض للتأكد بشكل صحيح من أي عوامل خطر مخفية محتملة قد تساهم في تطور تجاويف عظم الفك. على سبيل المثال، أحد الاعتبارات المهمة عند علاج تجاويف عظم الفك هو ما إذا كان الفرد يتناول مضادات الاكتئاب، وتحديدًا مثبطات إعادة امتصاص السيروتونين الانتقائية (SSRIs). ارتبطت مثبطات استرداد السيروتونين الانتقائية بانخفاض كثافة كتلة العظام وزيادة معدلات الكسور. يمنع SSRI Fluoxetine (Prozac) بشكل مباشر تمايز الخلايا العظمية والتمعدن. أظهرت دراستان مستقلتان على الأقل فحصتا مستخدمي SSRI مقارنة بالضوابط أن استخدام SRRI يرتبط بمؤشرات مورفومترية بانورامية أسوأ.
قد تساهم الشروط المسبقة أيضًا في نتائج العلاج الناجحة. يتضمن ذلك خلق بيئة نسيجية تساعد على الشفاء من خلال تزويد الجسم بمستويات كافية من العناصر الغذائية المناسبة التي تعمل على تحسين التضاريس البيولوجية عن طريق تحسين التوازن في الجسم. إن تكتيكات الشروط المسبقة ليست ممكنة دائمًا، أو مقبولة للمريض، ولكنها أكثر أهمية بالنسبة للمرضى الذين لديهم قابليات معروفة، مثل أولئك الذين لديهم استعداد وراثي، أو اضطرابات الشفاء أو صحة معرضة للخطر. في مثل هذه الحالات، من الأهمية بمكان أن يحدث هذا التحسين لتقليل مستويات الإجهاد التأكسدي، والذي لا يمكن أن يحفز عملية المرض فحسب، بل يمكن أن يتداخل مع الشفاء المطلوب.
من الناحية المثالية، يجب الانتهاء من تقليل أي حمل سام على الجسم مثل الفلورايد و/أو الزئبق من حشوات ملغم الأسنان قبل علاج تجاويف عظم الفك. يمكن للزئبق أن يحل محل الحديد في سلسلة نقل الإلكترون في الميتوكوندريا. يؤدي هذا إلى زيادة الحديد الحر (الحديد الحديدي أو Fe++)، مما ينتج عنه أنواع أكسجين تفاعلية ضارة (ROS) تُعرف أيضًا باسم الجذور الحرة، والتي تسبب الإجهاد التأكسدي. كما أن الحديد الزائد في أنسجة العظام يمنع أيضًا الوظيفة المناسبة للخلايا العظمية، والتي من الواضح أنه سيكون لها تأثير سلبي عند محاولة شفاء اضطراب العظام.
وينبغي أيضا معالجة أوجه القصور الأخرى قبل العلاج. عندما يكون هناك نقص في النحاس والمغنيسيوم والريتينول المتوفر بيولوجيًا، يصبح التمثيل الغذائي وإعادة تدوير الحديد غير منظم في الجسم، مما يساهم في زيادة الحديد الحر في الأماكن الخاطئة مما يؤدي إلى زيادة الإجهاد التأكسدي وخطر الإصابة بالأمراض. وبشكل أكثر تحديدًا، تصبح العديد من الإنزيمات في الجسم (مثل السيرولوبلازمين) غير نشطة عندما تكون هناك مستويات غير كافية من النحاس والمغنيسيوم والريتينول المتوفر بيولوجيًا، مما يؤدي بعد ذلك إلى إدامة خلل تنظيم الحديد النظامي وما ينتج عن ذلك من زيادة في الإجهاد التأكسدي وخطر الإصابة بالأمراض.
وينبغي أيضًا تقييم التقنيات البديلة المستخدمة كعلاجات أولية أو داعمة. وتشمل هذه المعالجة المثلية، والتحفيز الكهربائي، والعلاج بالضوء مثل التعديل الحيوي الضوئي، والليزر، والأكسجين الطبي / الأوزون، والأكسجين عالي الضغط، وطرائق منع تخثر الدم، وعلاجات سانوم، والتغذية والمغذيات، والساونا بالأشعة تحت الحمراء، والعلاج بالأوزون عن طريق الوريد، وعلاجات الطاقة، وغيرها. في هذا الوقت، لم يتم إجراء أي علم يؤكد أن هذه الأشكال البديلة من العلاج قابلة للتطبيق أو غير فعالة. وينبغي وضع معايير الرعاية لضمان الشفاء السليم وإزالة السموم. وينبغي اختبار تقنيات تقييم النجاح وتوحيدها. يجب وضع بروتوكولات أو إجراءات للمساعدة في تحديد متى يكون العلاج مناسبًا ومتى لا يكون مناسبًا للتقييم.
أظهرت الأبحاث أن وجود تجاويف في عظم الفك هو عملية مرضية خبيثة مرتبطة بانخفاض تدفق الدم. يؤدي ضعف تدفق الدم النخاعي إلى ضعف تمعدن الأوعية الدموية وعدم كفاية الأوعية الدموية في مناطق عظم الفك التي يمكن أن تصاب بمسببات الأمراض، مما يعزز الموت الخلوي. يتحدى تدفق الدم البطيء داخل آفات التجويف توصيل المضادات الحيوية والمواد المغذية والرسائل المناعية. يمكن للبيئة الإقفارية أيضًا أن تؤوي وتعزز وسطاء الالتهابات المزمنة التي قد يكون لها تأثيرات ضارة أكثر على الصحة الجهازية. الاستعداد الوراثي، وانخفاض وظائف المناعة، وتأثيرات بعض الأدوية، والصدمات النفسية والالتهابات، وعوامل أخرى مثل التدخين يمكن أن تحفز أو تسرع تطور تجاويف عظم الفك.
بالتعاون مع أخصائي علم أمراض عظم الفك البارز، الدكتور جيري بوكوت، يقدم IAOMT ويروج لتحديد صحيح من الناحية النسيجية والمرضية لآفات تجويف عظم الفك باعتبارها مرض نقص تروية النخاع المزمن في عظم الفك، CIMDJ. على الرغم من أن العديد من الأسماء والمختصرات والمصطلحات استخدمت تاريخيًا وتستخدم حاليًا للإشارة إلى هذا المرض، فإن IAOMT مقتنعة بأن هذا هو المصطلح الأكثر ملاءمة لوصف الحالة المرضية والنسيجية الدقيقة الموجودة بشكل شائع في تجاويف عظم الفك.
على الرغم من صعوبة تشخيص معظم آفات تجويف عظم الفك باستخدام الصور الشعاعية الروتينية ومعظمها غير مؤلمة، إلا أنه لا ينبغي للمرء أبدًا افتراض عدم وجود عملية المرض. هناك العديد من العمليات المرضية التي يصعب تشخيصها، والعديد منها غير مؤلم. إذا استخدمنا الألم كمؤشر للعلاج، فإن أمراض اللثة والسكري ومعظم أنواع السرطان لن يتم علاجها. يمتلك ممارس طب الأسنان اليوم مجموعة واسعة من الطرق لعلاج تجاويف عظم الفك بنجاح، كما أن الفشل في التعرف على المرض والتوصية بالعلاج لا يقل خطورة عن الفشل في تشخيص وعلاج أمراض اللثة. من أجل صحة ورفاهية مرضانا، يعد التحول النموذجي أمرًا بالغ الأهمية لجميع المتخصصين في الرعاية الصحية، بما في ذلك ممارسي طب الأسنان والطب، من أجل 1) التعرف على مدى انتشار تجاويف عظم الفك و2) الاعتراف بالصلة بين تجاويف عظم الفك والأمراض الجهازية.
نتائج مسح IAOMT 2 (2023)
كما تمت مناقشته بإيجاز في الورقة، فإن الحالات غير ذات الصلة غالبًا ما تتحسن بعد جراحة التجويف. لمعرفة المزيد حول أنواع الحالات التي يتم علاجها وكيفية حدوث الهدأة القريبة فيما يتعلق بالجراحة، تم إرسال استطلاع ثانٍ إلى أعضاء IAOMT. تم تجميع قائمة بالأعراض والحالات التي لاحظ أعضاء هذه اللجنة تحسنها بعد الجراحة من أجل المسح. تم سؤال المشاركين عما إذا كانوا قد لاحظوا عودة أي من هذه الحالات بعد الجراحة، وإذا كان الأمر كذلك إلى أي درجة. وسُئلوا أيضًا عما إذا كانت الأعراض قد اختفت بسرعة أو إذا استغرق التحسن وقتًا أطول من شهرين. بالإضافة إلى ذلك، تم سؤال المشاركين عما إذا كانوا يقومون عادة بإجراء عملية جراحية في مواقع فردية، أو مواقع أحادية متعددة، أو جميع المواقع في عملية جراحية واحدة. وترد نتائج الاستطلاع في الأشكال أدناه. البيانات أولية، نظراً لأن عدد المشاركين كان صغيراً (33) وأن هناك بعض البيانات الناقصة.
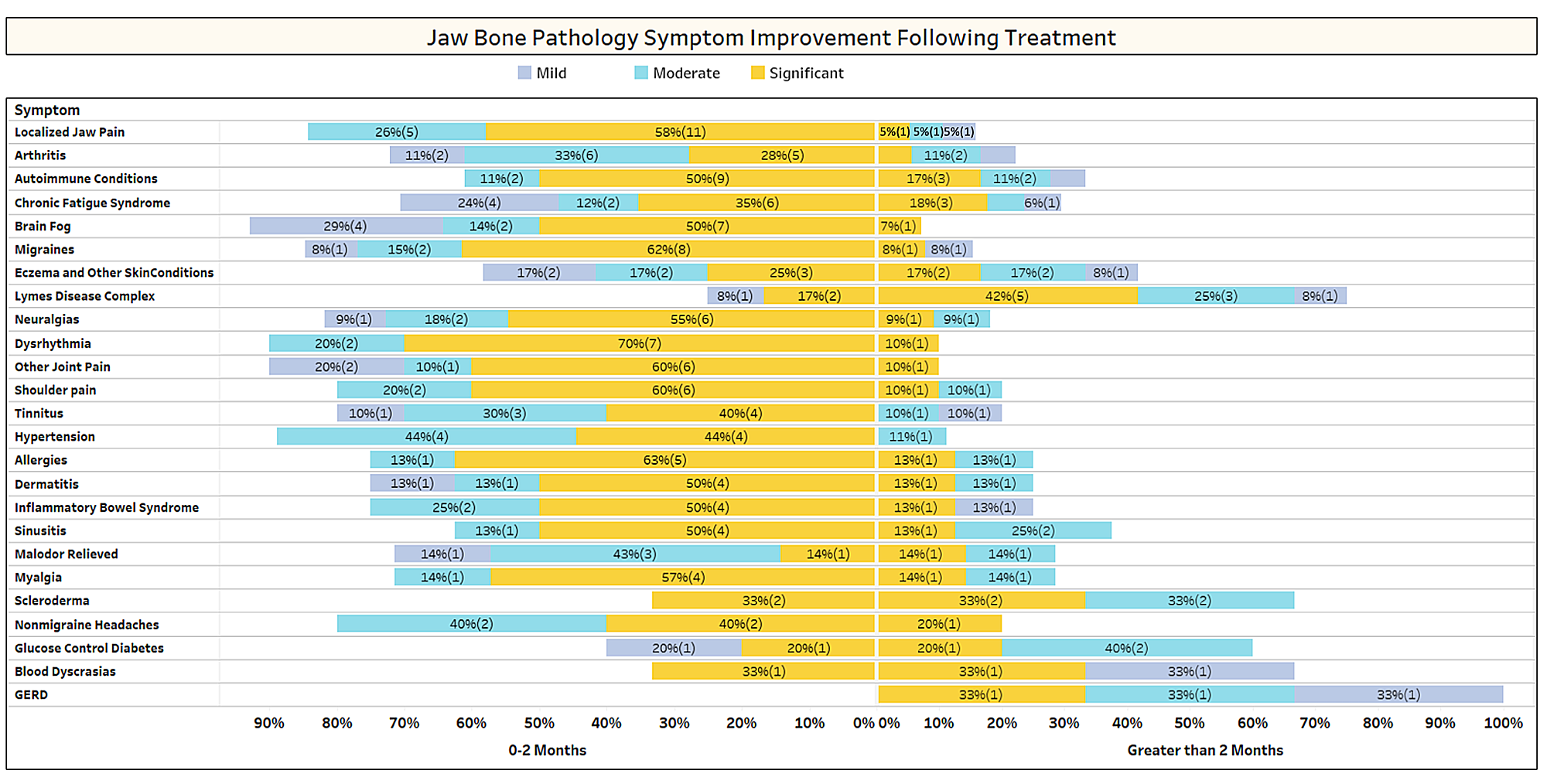
الملحق الأول الشكل 1 قام المشاركون بتقييم مستوى التحسن (معتدل أو متوسط أو كبير) ولاحظوا ما إذا كان التحسن قد حدث بسرعة (0-2 أشهر) أو استغرق وقتًا أطول (> شهرين). يتم سرد الحالات/الأعراض حسب ترتيب الأكثر الإبلاغ عنها. لاحظ أن معظم الحالات/الأعراض تختفي في أقل من شهرين (الجانب الأيسر من خط الوسط).
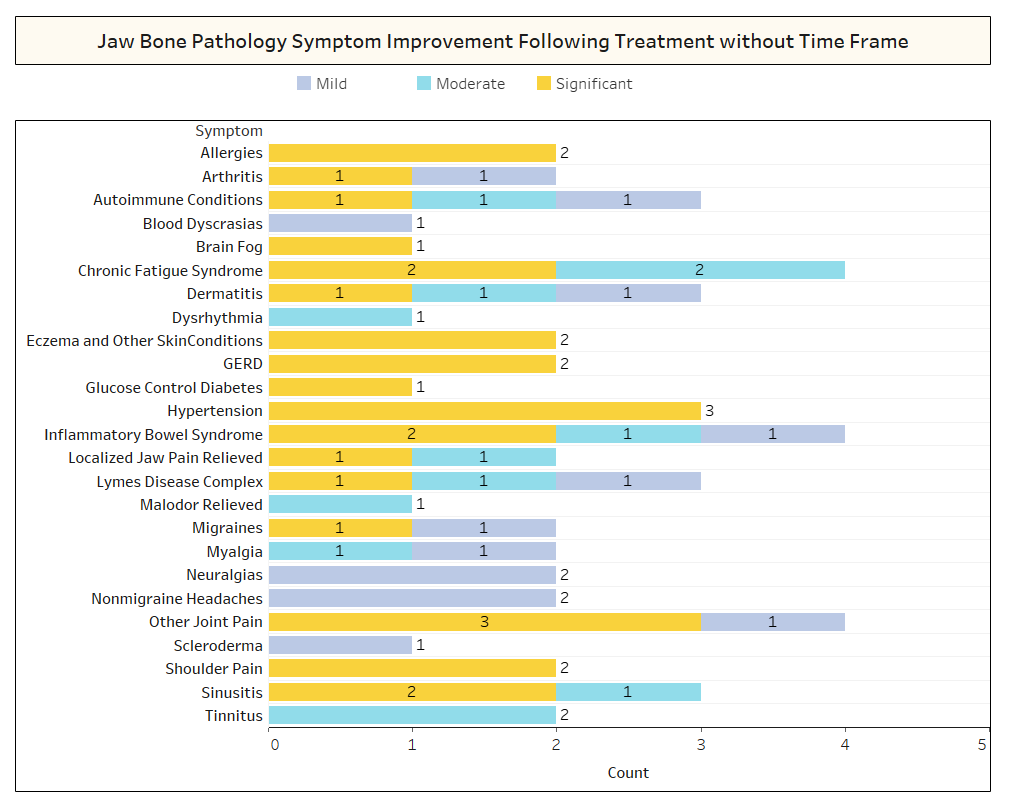
الملحق الأول الشكل 2 كما هو موضح أعلاه، في العديد من الحالات، لم يلاحظ المشاركون الإطار الزمني للتعافي من التحسينات التي تمت ملاحظتها.
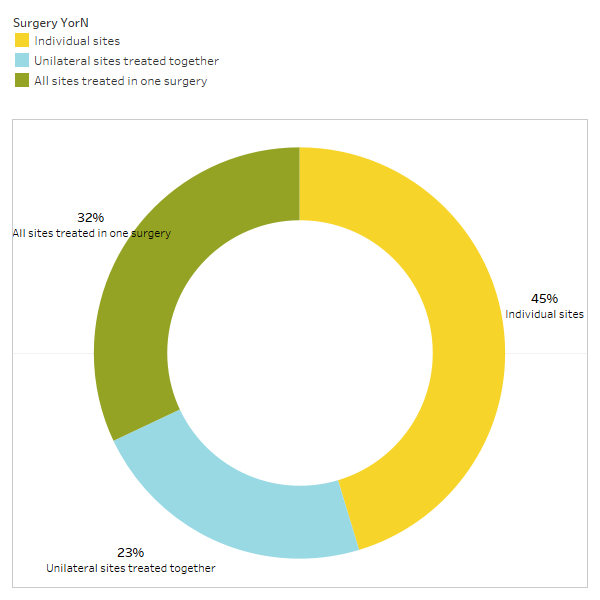
الملحق الأول الشكل 3 أجاب المشاركون على السؤال: "هل توصي/تؤدي عادةً؟
عملية جراحية لمواضع فردية، أو معالجة المواقع الأحادية معًا، أو معالجة جميع المواقع في عملية واحدة؟
نتائج مسح IAOMT 1 (2021)
نظرًا لندرة الأدبيات ومراجعات الحالات السريرية المتعلقة بمعالجة آفات التجويف، قامت IAOMT باستقصاء أعضائها لجمع المعلومات المتعلقة بالاتجاهات والعلاجات التي تتطور نحو "معيار الرعاية". الاستطلاع الكامل متاح على موقع IAOMT (لاحظ أنه لم يستجب جميع الممارسين لجميع استفسارات الاستطلاع).
لتلخيص ذلك بإيجاز، فإن غالبية المشاركين الـ 79 يقدمون العلاج الجراحي، والذي يتضمن انعكاس الأنسجة الرخوة، والوصول الجراحي لموقع التجويف، وطرق مختلفة "للتنظيف" الجسدي وتطهير الموقع المصاب. يتم استخدام مجموعة واسعة من الأدوية والمغذيات و/أو منتجات الدم لتعزيز شفاء الآفة قبل إغلاق شق الأنسجة الرخوة.
غالبًا ما تستخدم الأزيز الدوارة لفتح الآفة العظمية أو الوصول إليها. يستخدم معظم الأطباء أداة يدوية لكشط أو كشط العظام المريضة (68%)، ولكن يتم أيضًا استخدام تقنيات وأدوات أخرى، مثل المثقاب الدوار (40%)، أو أداة كهرضغطية (فوق صوتية) (35%) أو ليزر ER:YAG (36%)، وهو تردد ليزر يستخدم للبث الصوتي الضوئي.
بمجرد تنظيف الموقع و/أو تنضيره و/أو كشطه، يستخدم معظم المشاركين ماء/غاز الأوزون لتطهير وتعزيز الشفاء. 86% من المشاركين يستخدمون PRF (الفيبرين الغني بالصفائح الدموية)، أو PRP (البلازما الغنية بالصفائح الدموية) أو PRF أو PRP بالأوزون. إحدى تقنيات التطهير الواعدة المذكورة في الأدبيات وفي هذا الاستطلاع (42%) هي استخدام Er:YAG أثناء العملية الجراحية. 32% من المشاركين لا يستخدمون أي نوع من الطعوم العظمية لملء موقع التجويف.
معظم المشاركين (59٪) عادة لا يقومون بأخذ خزعة للآفات موضحين مجموعة متنوعة من الأسباب من التكلفة، أو عدم القدرة على الحصول على عينات أنسجة قابلة للحياة، أو صعوبة العثور على مختبر علم الأمراض، أو التأكد من حالة المرض.
لا يستخدم معظم المشاركين المضادات الحيوية قبل الجراحة (79%)، أو أثناء الجراحة (95%)، أو بعد الجراحة (69%). يشمل الدعم الوريدي الآخر المستخدم ستيرويدات الديكساميثازون (8٪) والفيتامينات C (48٪). يستخدم العديد من المشاركين (52%) العلاج بالليزر منخفض المستوى (LLLT) بعد العملية الجراحية لأغراض الشفاء. يوصي العديد من المشاركين بدعم المغذيات بما في ذلك الفيتامينات والمعادن والعديد من العلاجات المثلية قبل (81٪) وأثناء (93٪) فترة الشفاء.
 الصور
الصور
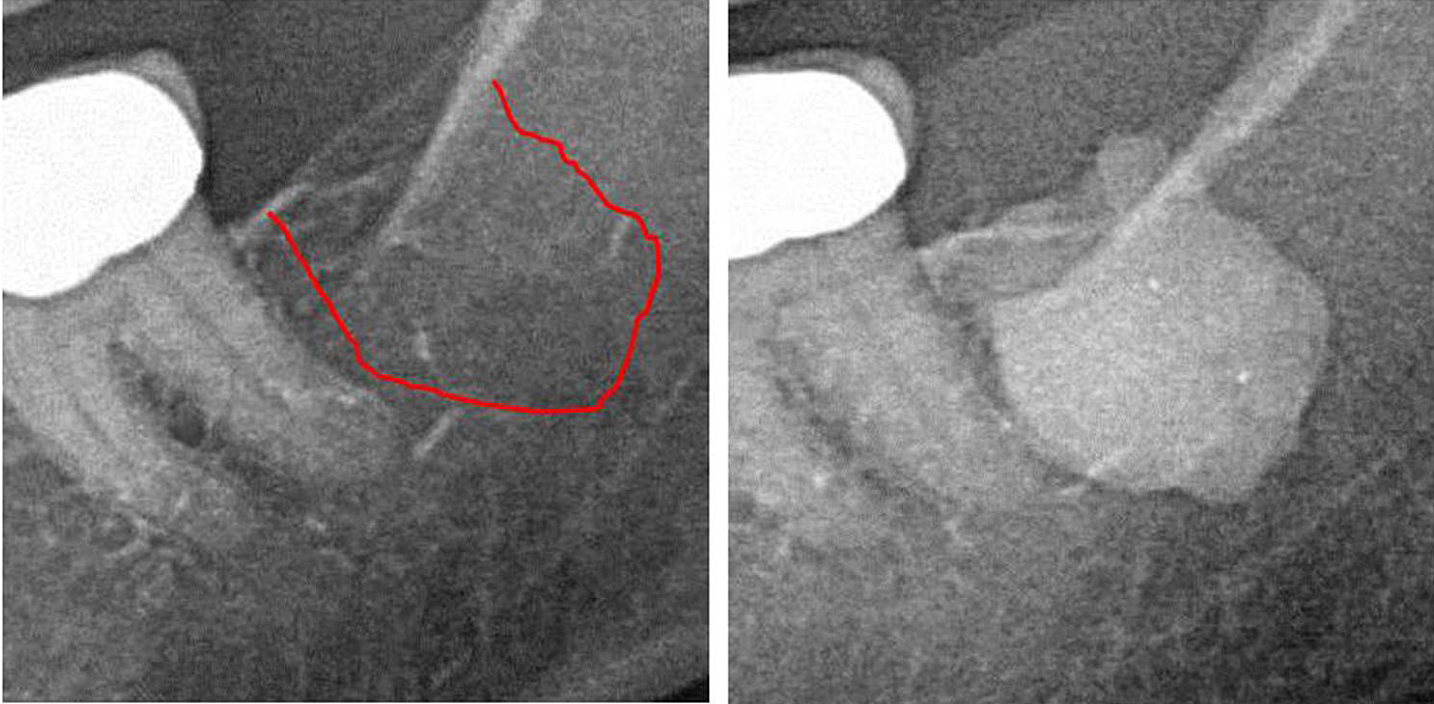
الملحق الثالث الشكل 1 اللوحة اليسرى: تشخيصات الأشعة السينية ثنائية الأبعاد للمنطقة رقم 2. اللوحة اليمنى: توثيق اتساع FDO) في المنطقة خلف الرحى 38/38 باستخدام عامل تباين بعد جراحة FDOJ.
الاختصارات: FDOJ، تنخر العظم التنكس الدهني في عظم الفك.
مقتبس من Lechner، وآخرون، 2021. "تجويف عظم الفك المُعبَّر عن RANTES/CCL5: دراسات حالة تربط الالتهاب الصامت في عظم الفك بنظرية المعرفة حول سرطان الثدي." سرطان الثدي: الأهداف والعلاج
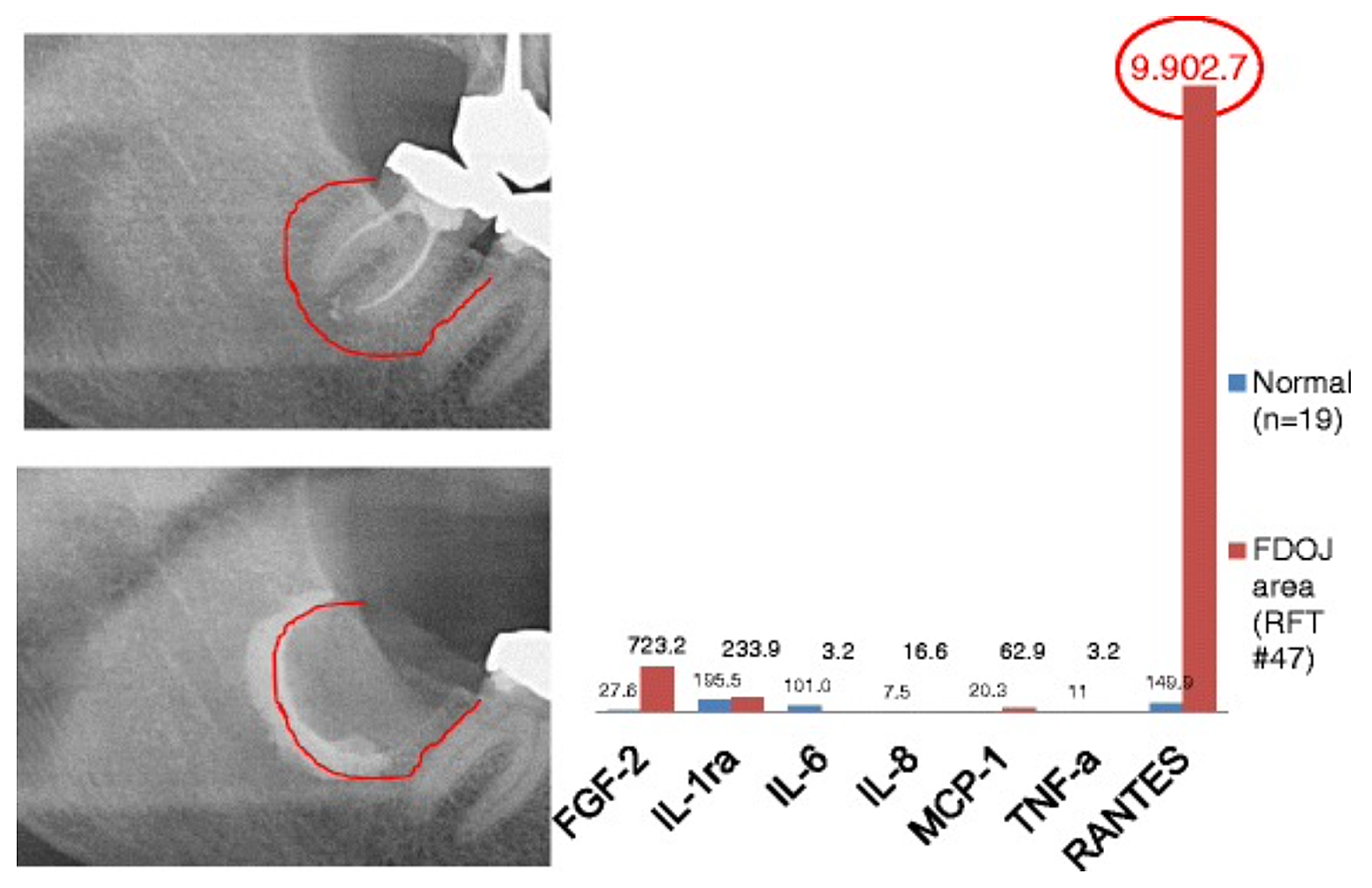
الملحق 3 الشكل 2 مقارنة سبعة السيتوكينات (FGF-2، IL-1ra، IL-6، IL-8، MCP-1، TNF-a و RANTES) في FDOJ تحت RFT # 47 مع السيتوكينات في عظم الفك الصحي (n = 19). التوثيق أثناء العملية الجراحية لتمديد FDOJ في عظم الفك السفلي الأيمن، المنطقة رقم 47 من RFT #47، بواسطة عامل التباين بعد الإزالة الجراحية لـ RFT #47.
الاختصارات: FDOJ، تنخر العظم التنكس الدهني في عظم الفك.
مقتبس من Lechner وvon Baehr, 2015. "Chemokine RANTES/CCL5 كحلقة وصل غير معروفة بين التئام الجروح في عظم الفك والأمراض الجهازية: هل التنبؤ والعلاجات المصممة في الأفق؟" مجلة EPMA
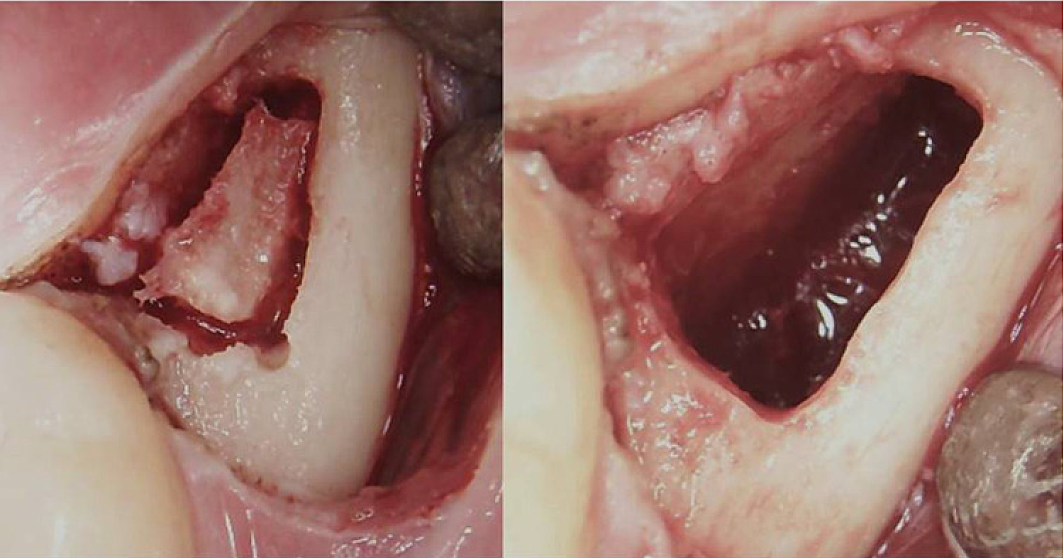
الملحق الثالث الشكل 3 إجراء جراحي لـ BMDJ/FDOJ خلف الرحى. اللوحة اليسرى: بعد طي السديلة المخاطية السمحاقية، تم تشكيل نافذة عظمية في القشرة. اللوحة اليمنى: تجويف النخاع مجعد.
الاختصارات: BMDJ، خلل في نخاع العظم في عظم الفك. FDOJ، تنخر العظم التنكس الدهني في عظم الفك.
مقتبس من Lechner وآخرون، 2021. "متلازمة التعب المزمن وعيوب نخاع العظم في الفك - تقرير حالة عن التشخيص الإضافي للأشعة السينية للأسنان باستخدام الموجات فوق الصوتية." مجلة تقارير الحالة الطبية الدولية
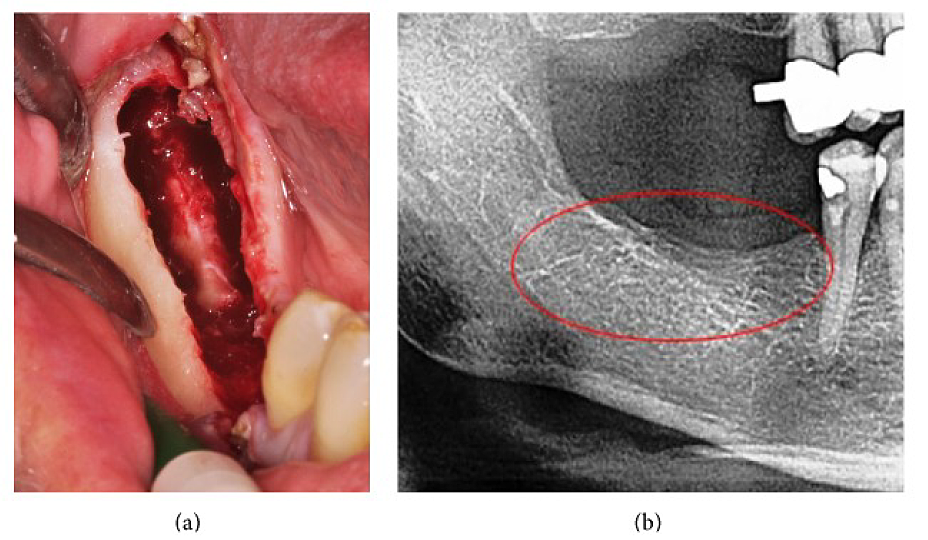
الملحق الثالث الشكل 4 ( أ ) كشط FDOJ في الفك السفلي باستخدام العصب السنخي تحت العاري. (ب) الأشعة السينية المقابلة دون أي علامات للعملية المرضية في عظم الفك.
الاختصارات: FDOJ، تنخر العظم التنكس الدهني في عظم الفك
مقتبس من Lechner، وآخرون، 2015. "ألم الاعتلال العصبي المحيطي الوجهي/ألم مثلث التوائم وRANTES/CCL5 في تجويف عظم الفك." المبنية على الأدلة التكميلي والطب البديل
فيلم Appx III 1
مقطع فيديو (انقر نقرا مزدوجا على الصورة لمشاهدة المقطع) لعملية جراحية لعظم الفك تظهر كريات دهنية وإفرازات قيحية من عظم الفك لمريض يشتبه في إصابته بنخر في عظم الفك. بإذن من الدكتور ميغيل ستانلي، DDS
فيلم Appx III 2
مقطع فيديو (انقر نقرا مزدوجا على الصورة لمشاهدة المقطع) لعملية جراحية لعظم الفك تظهر كريات دهنية وإفرازات قيحية من عظم الفك لمريض يشتبه في إصابته بنخر في عظم الفك. بإذن من الدكتور ميغيل ستانلي، DDS
لتنزيل هذه الصفحة أو طباعتها بلغة مختلفة، اختر لغتك من القائمة المنسدلة الموجودة في الجزء العلوي الأيسر أولاً.
ورقة موقف IAOMT حول مؤلفي تجاويف عظم الفك البشري













